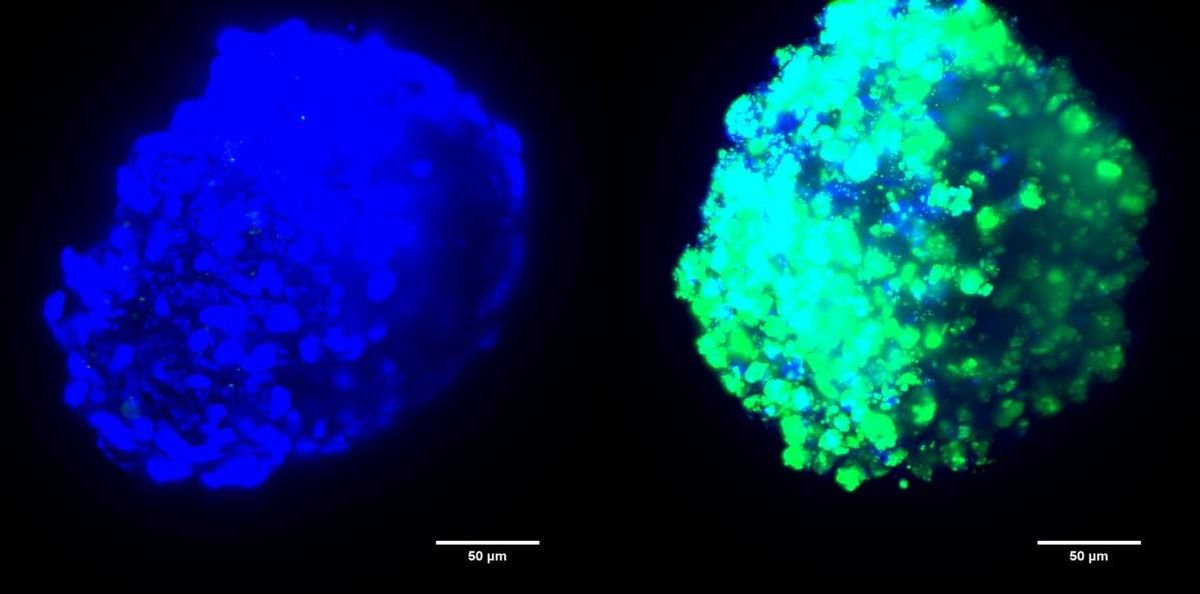
Os resultados desta terapia, ensaiada con Ă©xito en tumores humanos implantados en ratos, foron publicados na revista ÂAdvanced TherapeuticsÂ.
O tratamento actual para o tumor cerebral mĂĄis comĂșn e letal, o glioblastoma multiforme (GBM), basĂ©ase fundamentalmente na cirurxĂa de extirpaciĂłn, e acada unha supervivencia media de pouco mĂĄis de 14 meses Âa supervivencia aos cinco anos Ă© menor do 5%Â. Malia todo, esta situaciĂłn poderĂa mellorar grazas a un novo tratamento desenvolvido por un equipo dirixido polo cientĂfico Marcos GarcĂa Fuentes, investigador do Centro de InvestigaciĂłn en Medicina Molecular e Enfermidades CrĂłnicas (CiMUS) da Universidade de Santiago, quen recibiu o apoio dunha Axuda a Equipos de InvestigaciĂłn en Biomedicina da FundaciĂłn BBVA. O equipo do doutor GarcĂa Fuentes, en colaboraciĂłn co Instituto de SaĂșde Carlos III e a Universidade de Nottingham, logrou desenvolver nanopartĂculas capaces de penetrar tumores cerebrais e transportar fĂĄrmacos xenĂ©ticos ata o interior das cĂ©lulas cancerĂxenas. A tĂ©cnica tense ensaiado xa con Ă©xito en ratos, nun experimento cuxos resultados publica a revista Advanced Therapeutics.
A utilizaciĂłn de medicamentos capaces de silenciar xenes causantes de tumores ten un enorme potencial para o desenvolvemento de terapias especĂficas, personalizadas e efectivas no tratamento do cancro. Non obstante, estes medicamentos xenĂ©ticos non teñen aĂnda unha ampla aplicaciĂłn, debido aos seus grandes problemas de estabilidade e transporte no corpo. Por exemplo, sĂĄbese que cando unha cĂ©lula exponse a secuencias de fĂĄrmacos xenĂ©ticos, menos dunha de cada cen das devanditas secuencias terapĂ©uticas conseguirĂĄ chegar ao interior de cĂ©lula para exercer a sĂșa acciĂłn. Este complexo camiño cara o interior celular dĂ©bese a que os medicamentos xenĂ©ticos son internalizados a travĂ©s de vesĂculas dixestivas, que degradan o seu contido.
Agora, o equipo dirixido polo doutor GarcĂa Fuentes vĂ©n de ensaiar o uso de novos nanomateriais (denominados polifosfacenos), como vehĂculos capaces de mellorar o transporte dos medicamentos xenĂ©ticos contra o cancro. O estudo destes materiais permitiu identificar un derivado que non sĂł reduce de xeito moi significativo a toxicidade dos tratamentos, senĂłn que mellora o seu transporte no camiño ao interior das cĂ©lulas e a sĂșa penetraciĂłn en tumores. «O segredo deste material Âexplica GarcĂa Fuentes- Ă© unha estrutura que se volve Âinsoluble na contorna ĂĄcida das vesĂculas dixestivas, inducindo a sĂșa desestabilizaciĂłn e permitindo ao medicamento xenĂ©tico Âescapar ao interior celular».
A travĂ©s dunha colaboraciĂłn con investigadores do Instituto de SaĂșde Carlos III, as nanopartĂculas terapĂ©uticas foron cargadas cunha secuencia capaz de suprimir cĂ©lulas iniciadoras do glioblastoma multiforme. O estudo, realizado en tumores humanos implantados en ratos, mostrou que a aplicaciĂłn do medicamento xenĂ©tico, en combinaciĂłn coa quimioterapia de primeira liña (temozolamida), produce unha reduciĂłn tumoral maior que un tratamento baseado unicamente no fĂĄrmaco quimioterĂĄpico.
ÂA Axuda da FundaciĂłn BBVA foi moi importante para nĂłs, xa que somos un laboratorio pequeno e sen ese financiamento non o poderĂamos ter levado a cabo; permitiunos seguir unha liña de investigaciĂłn na fronteira do coñecemento para aplicar esta terapia xĂ©nica e deunos unha meirande visibilidade, xa que se trata dunha axuda moi competitiva e destinada a investigaciĂłn de excelenciaÂ, salienta o investigador.
ImplantaciĂłn directa no cerebro
O obxectivo deste novo tratamento Ă© que se realice como complemento ĂĄ cirurxĂa de extirpaciĂłn e ao mesmo tempo que a quimioterapia, para conseguir que as cĂ©lulas tumorais non se reproduzan. «A idea Ă© implantala directamente no cerebro, por exemplo, aproveitando a extirpaciĂłn, porque a vĂa intravenosa Ă© moi complicada e ten menos probabilidades de Ă©xito; as probas con ratos deron resultados moi bos, como demostra o feito de que os ratos aos que sĂł se lles daba quimioterapia acababan con tumores o dobre de grandes que os que se trataban con quimioterapia e nanopartĂculas», apunta GarcĂa Fuentes.
O investigador engade que, aĂnda que ata que non realicen ensaios clĂnicos non o saberĂĄn con seguridade, os resultados preliminares indican que o efecto da terapia xĂ©nica vai estar limitado a unha ou dĂșas semanas, o que implicarĂa que o paciente deberĂa realizar ciclos do tratamento do mesmo xeito que se fai coa quimioterapia.
Actualmente, o equipo de investigaciĂłn dirixido por GarcĂa Fuentes estĂĄ a traballar en desenvolvementos mellorados da tecnoloxĂa, con vistas a chegar a acordos con empresas interesadas en impulsar o desenvolvemento clĂnico da tecnoloxĂa no futuro. «Se todo sae ben e logramos o apoio de empresas, poderiamos empezar a realizar os primeiros ensaios clĂnicos en pacientes dentro de catro ou cinco anos», asegura este cientĂfico. Ademais, considera que, unha vez verificada a sĂșa eficacia, a tĂ©cnica poderĂa utilizarse tamĂ©n para tratar outro tipo de tumores, como o melanoma.
 O presidente da Xunta, Alfonso Rueda, anunciou hoxe que a Xunta destinarĂĄ un total de 270 millĂłns de euros a paliar os efectos do conflito en Oriente Medio na nosa comunidade. Durante a sesiĂłn de control no Pleno do Parlamento de Galicia en resposta ĂĄs preguntas dos grupos parlamentarios, o titular do Goberno galego lembrou, ao respecto da situaciĂłn en Oriente Medio, que o Consello da Xunta xa analizou hai dĂșas semanas 'os primeiros impactos' e que Galicia foi 'a primeira comunidade autĂłnoma en falar cos clĂșsteres'. Nesta liña, o presidente anunciou que o vindeiro Consello autorizarĂĄ 'un plan de mĂĄis de 150 millĂłns' para atender aos sectores afectados, que se sumarĂĄ aos mĂĄis de 120 millĂłns que suporĂĄ para Galicia financiar as iniciativas do Goberno central a este respecto.
O presidente da Xunta, Alfonso Rueda, anunciou hoxe que a Xunta destinarĂĄ un total de 270 millĂłns de euros a paliar os efectos do conflito en Oriente Medio na nosa comunidade. Durante a sesiĂłn de control no Pleno do Parlamento de Galicia en resposta ĂĄs preguntas dos grupos parlamentarios, o titular do Goberno galego lembrou, ao respecto da situaciĂłn en Oriente Medio, que o Consello da Xunta xa analizou hai dĂșas semanas 'os primeiros impactos' e que Galicia foi 'a primeira comunidade autĂłnoma en falar cos clĂșsteres'. Nesta liña, o presidente anunciou que o vindeiro Consello autorizarĂĄ 'un plan de mĂĄis de 150 millĂłns' para atender aos sectores afectados, que se sumarĂĄ aos mĂĄis de 120 millĂłns que suporĂĄ para Galicia financiar as iniciativas do Goberno central a este respecto.
 Para a ediciĂłn de 2026, chegan desde o outro lado do AtlĂĄntico La Cura e El VacĂo (ambas estreas en España), nas que o coreĂłgrafo cubano Julio CĂ©sar Iglesias dirixe ĂĄ prestixiosa CompañĂa Colombiana de Danza ContemporĂĄnea. TamĂ©n a conferencia escĂ©nica Arder Ăpica (Cap. 1) na que o artista brasileiro Reinaldo Ribeiro constrĂșe unha nova memoria colectiva a partir das cinzas que deixou o incendio do Museo Nacional do Brasil en 2018. Forma parte tamĂ©n da programaciĂłn a instalaciĂłn inmersiva Hecatombe II: Movementos e rituais para a renovaciĂłn do mundo, da colombiana de orixe indĂxena Martha HincapiĂ© Charry, que rescata saberes ancestrais de lĂderes nativos das primeiras naciĂłns americanas.
Para a ediciĂłn de 2026, chegan desde o outro lado do AtlĂĄntico La Cura e El VacĂo (ambas estreas en España), nas que o coreĂłgrafo cubano Julio CĂ©sar Iglesias dirixe ĂĄ prestixiosa CompañĂa Colombiana de Danza ContemporĂĄnea. TamĂ©n a conferencia escĂ©nica Arder Ăpica (Cap. 1) na que o artista brasileiro Reinaldo Ribeiro constrĂșe unha nova memoria colectiva a partir das cinzas que deixou o incendio do Museo Nacional do Brasil en 2018. Forma parte tamĂ©n da programaciĂłn a instalaciĂłn inmersiva Hecatombe II: Movementos e rituais para a renovaciĂłn do mundo, da colombiana de orixe indĂxena Martha HincapiĂ© Charry, que rescata saberes ancestrais de lĂderes nativos das primeiras naciĂłns americanas.