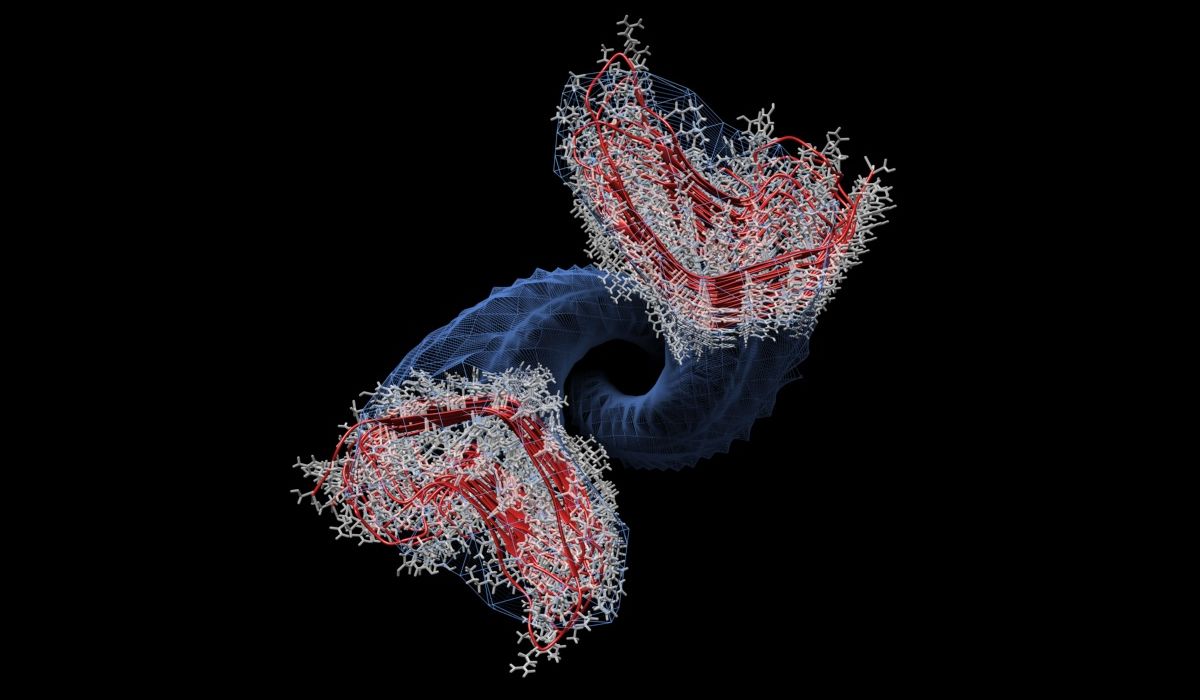
O grupo do profesor JesĂşs Requena, xunto con investigadores da Universidade de Trento (Italia) acaba de presentar un modelo computacional que revela os mecanismos da replicaciĂłn dos priĂłns, os axentes responsables das enfermidades das Âvacas tolas e os Âcervos zombisÂ. O estudo representa un importante avance no coĂąecemento destes enigmĂĄticos patĂłxenos que tamĂŠn afectan aos seres humanos, explica JesĂşs Requena, investigador do Centro Singular de InvestigaciĂłn en Medicina Molecular e Enfermidades CrĂłnicas da USC (CiMUS).
Nun artigo publicado na revista PLOS Pathogens, os investigadores presentan un Âmodelo computacional realista e fisicamente plausible da estrutura atĂłmica e o mecanismo de replicaciĂłn dos priĂłns, os axentes infecciosos responsables da enfermidade das vacas tolas e a consunciĂłn crĂłnica dos cĂŠrvidos, bautizada popularmente como Âenfermidade dos cervos zombisÂ, endĂŠmica en Norte AmĂŠrica e da que se rexistraron os primeiros casos recentemente en Europa. Os resultados obtidos son froito da colaboraciĂłn do grupo do profesor Requena e o de Emiliano Biasini, da Universidade de Trento.
Os priĂłns son Âaxentes patoxĂŠnicos e infecciosos inusuais, formados pola proteĂna PrPSc, unha variante aberrantemente pregada da proteĂna fisiolĂłxica PrPC, que existe nos cerebros de todos os mamĂferos e cuxa funciĂłn non estĂĄ ainda ben definidaÂ, explica JesĂşs Requena. Os priĂłns PrPSc replĂcanse en ausencia de material xenĂŠtico recrutando molĂŠculas de PrPC e forzĂĄndoas a mudar a sĂşa conformaciĂłn, ata convertelas en PrPSc. Como sinala o investigador da USC, a acumulaciĂłn de priĂłns PrPSc no sistema nervioso central estĂĄ na base de enfermidades neurodexenerativas mortais denominadas encefalopatĂas esponxiformes transmisibles, como a enfermidade de Creutzfeldt-Jakob e o insomnio familiar fatal nos seres humanos, ademais de na mencionada enfermidade das vacas tolas, que nos anos 90 afectou a centos de milleiros de bovinos de toda Europa, en particular no Reino Unido, e que se transmitiu a mais de 200 persoas.
Por outra banda e ĂĄ vista dos resultados obtidos, polo momento todas as investigaciĂłns suxiren que a enfermidade do cervo zombi non ĂŠ transmisible aos seres humanos aclara o doutor Requena, aĂnda que convĂŠn ter moita precauciĂłn xa que a travĂŠs da transmisiĂłn dunhas especies animais a outras (por exemplo, de cĂŠrvidos a cabras ou ovellas que compartan espazos naturais ou pastos), as propiedades dos priĂłns poden variar e as barreiras de transmisiĂłn, franquearse, especifica o investigador do CiMUS.
ColaboraciĂłn internacional e multidisciplinar
Partindo do coĂąecemento da arquitectura xeral do priĂłn, obtida mediante criomicroscopĂa electrĂłnica nun traballo previo tamĂŠn dirixido polo profesor Requena, xunto con datos bioquĂmicos adicionais, os grupos galego e italiano deseĂąaron un modelo molecular do priĂłn que resulta coherente con todos os datos experimentais dispoĂąibles ata o momento. Giovanni Spagnolli, do grupo de Trento, someteu o modelo a unha tĂŠcnica computacional denominada DinĂĄmica Molecular, para o que se precisou a utilizaciĂłn durante miles de horas dos recursos do supercomputador Finis Terrae do CESGA.
Estas anĂĄlises axudaron a refinar o modelo e determinaron que ĂŠ estable, en contraste con outros modelos propostos anteriormente, que se Âesfarelan na simulaciĂłn en poucos nanosegundos. Partindo deste modelo, o fĂsico da Universidade de Trento Pietro Faccioli aplicou un algoritmo fĂsico-matemĂĄtico desenvolvido polo seu equipo para predicir por primeira vez as transiciĂłns conformacionais que dan lugar ĂĄ transformaciĂłn da forma normal na forma aberrante da proteĂna priĂłnica. ÂA multidisciplinaridade foi a chave deste traballo, sen a colaboraciĂłn de expertos en bioquĂmica de proteĂnas, bioinformĂĄtica e fĂsica de distintas instituciĂłns e mesmo paĂses, as ideas, datos e cĂĄlculos necesarios para simular un proceso tan complexo non terĂan sido posibles. Por primeira vez temos reconstruĂdo un mecanismo fisicamente plausible da replicaciĂłn do priĂłnÂ, afirmou Giovanni Spagnolli, primeiro autor de traballo.
ÂSorprendentemente, os fundamentos quĂmicos que Âemprega o priĂłn para propagarse, como a formaciĂłn duns enlaces denominados Âpontes de hidrĂłxenoÂ, son moi similares aos que estĂĄn en xogo na propagaciĂłn do ADN; sĂł que poderĂa dicirse que a copia do priĂłn ĂŠ un proceso ÂanalĂłxico e a do ADN ÂdixitalÂ, por iso os nosos xenes estĂĄn feitos de ADN e non de priĂłns. comentou pola sĂşa banda JesĂşs Requena, coordinador e Ăşltimo asinante do traballo. O investigador da USC engade que aĂnda sendo moi informativo, a estrutura presentada ĂŠ un modelo, e a Ăşnica forma de saber canto se aproxima ĂĄ estrutura real do priĂłn PrPSc ĂŠ utilizando mĂŠtodos experimentais, como a Resonancia MagnĂŠtica Nuclear de estado sĂłlido, un proxecto no que o seu grupo, en colaboraciĂłn con Manuel MartĂn Pastor, do CACTUS, e VĂctor SĂĄnchez Pedregal, do CIQUS, xa estĂĄn traballando dende hai uns meses. O modelo foi presentado o mes pasado no congreso internacional Prion 2019, celebrado en Edmonton (CanadĂĄ), onde foi acollido con grande interese pola comunidade investigadora. Compre lembrar que Prion 2108 se celebrou e ano pasado en Santiago de Compostela baixo os auspicios da USC.
 Coralinda ĂŠ unha comedia xestual dirixida a pĂşblico familiar e infantil. A travĂŠs dunha linguaxe xestual fundamentada na manipulaciĂłn de obxectos e na interacciĂłn constante co dispositivo escĂŠnico, a obra constrĂşe un universo cĂłmico e poĂŠtico que transita do realismo ĂĄ hipĂŠrbole da vida cotiĂĄ. Unha proposta escĂŠnica ao estilo dos debuxos animados que aborda a temĂĄtica da inmigraciĂłn e do medio ambiente desde o humor, a poesĂa visual e a emociĂłn. A obra convida a reflexionar sobre as experiencias das persoas que viaxan lonxe da sĂşa terra.
Coralinda ĂŠ unha comedia xestual dirixida a pĂşblico familiar e infantil. A travĂŠs dunha linguaxe xestual fundamentada na manipulaciĂłn de obxectos e na interacciĂłn constante co dispositivo escĂŠnico, a obra constrĂşe un universo cĂłmico e poĂŠtico que transita do realismo ĂĄ hipĂŠrbole da vida cotiĂĄ. Unha proposta escĂŠnica ao estilo dos debuxos animados que aborda a temĂĄtica da inmigraciĂłn e do medio ambiente desde o humor, a poesĂa visual e a emociĂłn. A obra convida a reflexionar sobre as experiencias das persoas que viaxan lonxe da sĂşa terra.
 Foi presentadoo o novo festival Sons de Vigo que se celebrarĂĄ do 27 de marzo ao 4 de abril no Ifevi. Este evento aposta tanto por grandes nomes do panorama nacional como por artistas locais da escena galega. A presentaciĂłn, celebrada no Paseo das Avenidas, xunto ao monumento a Julio Verne como un dos sĂmbolos de Vigo, contou coa actuaciĂłn de Castle e Milutxo, mĂşsicos locais que ofreceron varios dos seus temas. Sons de Galicia forma parte da programaciĂłn dos Concertos do Xacobeo organizados pola Xunta de Galicia, unha iniciativa que impulsa a celebraciĂłn de grandes citas musicais en Galicia. O ciclo comezarĂĄ o 27 de marzo con Lingua Urbana, un dos cinco eventos musicais que acollerĂĄ o Ifevi dentro desta programaciĂłn.
Foi presentadoo o novo festival Sons de Vigo que se celebrarĂĄ do 27 de marzo ao 4 de abril no Ifevi. Este evento aposta tanto por grandes nomes do panorama nacional como por artistas locais da escena galega. A presentaciĂłn, celebrada no Paseo das Avenidas, xunto ao monumento a Julio Verne como un dos sĂmbolos de Vigo, contou coa actuaciĂłn de Castle e Milutxo, mĂşsicos locais que ofreceron varios dos seus temas. Sons de Galicia forma parte da programaciĂłn dos Concertos do Xacobeo organizados pola Xunta de Galicia, unha iniciativa que impulsa a celebraciĂłn de grandes citas musicais en Galicia. O ciclo comezarĂĄ o 27 de marzo con Lingua Urbana, un dos cinco eventos musicais que acollerĂĄ o Ifevi dentro desta programaciĂłn.